- 首页
- 关于我们
-
产品中心
- 光片显微镜系列
- LS-COMPACT光片显微镜 LS18平铺光片显微镜 锘海组织透明化底透台 透明度检测仪 组织透明化染色仪 高频震动切片机 活体循环系统 AMIRA三维视图和分析软件 高速固态硬盘
- 透明化试剂盒系列
- 组织透明化试剂盒(亲水型) 组织膨胀试剂盒 胚胎透明化试剂盒 增强型组织透明化试剂盒 细胞膨胀试剂盒 皮肤透明化试剂盒 组织切片透明&膨胀试剂盒(试用装) 骨组织透明化试剂盒 上皮或结缔类组织透明化试剂盒 非固定形态类软组织透明化试剂盒 肿瘤或致密组织透明化试剂盒 颅骨-脑组织透明化试剂盒 植物透明化试剂盒 活体颅骨透明化试剂盒 整鼠透明化试剂盒 Lectin血管标记物 PBS缓冲液 4%多聚甲醛固定液(PFA)
- 组织透明化及成像服务
- 单细胞空间多组学与高通量蛋白质组学科研检测服务 一站式科研服务——组织透明化、免疫染色、3D成像、数据分析及存储
- 小动物活体成像
- 小动物近红外二区成像
- 纳米药物制备系统/服务
- 微流控纳米药物递送平台 纳米药物载体合成服务
- 超快超分辨功能超声成像系统
- 超快超分辨功能超声成像系统
- 活体多光子及高分辨显微成像系统
- 高分辨率显微成像系统 双光子荧光寿命计数系统 活体多光子显微成像系统
- 试剂耗材
- 抗体系列产品 GATTA 显微镜纳米标尺 RISystem小鼠骨钉 Cellendes细胞水凝胶
- 小动物灌注/灌流设备
- 小动物灌注系统 灌流设备及附件
- 类器官3D细胞培养
- 锘海类器官、3D细胞培养系统
- 生物3D打印设备
- RegenHU生物3D打印机
-
应用案例
- 成像视频
- 成像视频
- 成像图片
- 成像图片
- 新闻资讯
- 联系我们
LNP配方新设计:阳离子两亲性药物选择性替代胆固醇
发布日期:2024/8/15 15:00:01
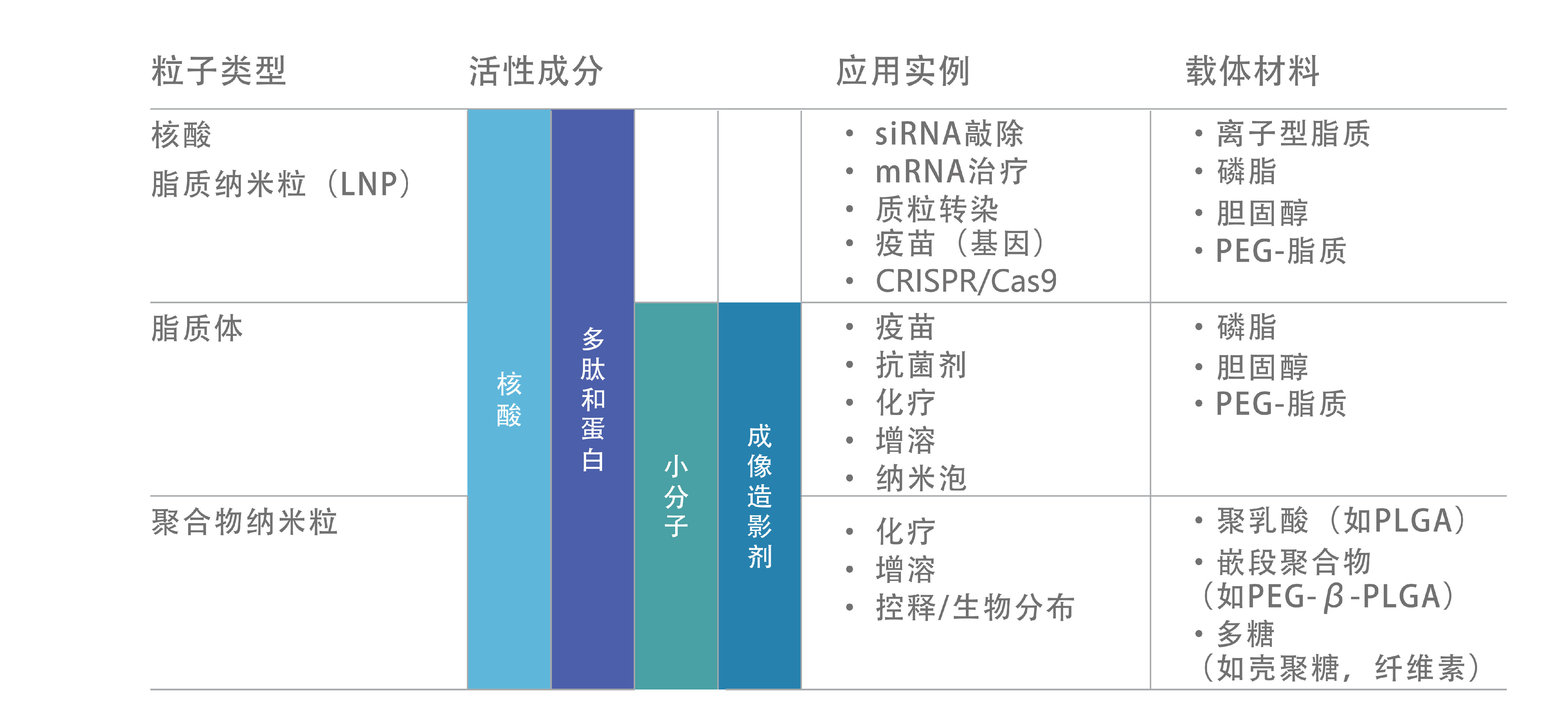
核酸脂质纳米粒(Lipid nanoparticle,LNP)已经成为一个成熟的递送平台,用于封装、保护各种核酸,递送至细胞质中。LNP经典配方如Onpattro、Comirnaty、SpikeVax,通常由四种脂质成分组成:可电离阳离子脂质、辅助性脂质、胆固醇、聚乙二醇(PEG)脂质,每种脂质都具有特定的功能(脂质纳米颗粒中各成分的作用)。
阳离子两亲性药物(Cationic amphiphilic drugs,CADs)是具有可电离脂类特征的多种药理学化合物,如去甲替林(NT)、氟伏沙明(Fluv)、氟西汀(Fluox)和地氯雷他定(DES),可以通过库仑相互作用或范德华力与脂质膜相互作用,改变脂质双分子层的性质。在本文中,作者使用CAD作为经典LNP配方的第五种成分,部分替代胆固醇,通过微流控设备进行合成,可以提升siRNA和mRNA在细胞质中的递送。合成的LNP雾化后,可以穿过人原代支气管上皮细胞产生粘液的气液界面模型中的粘液层。此外,在小鼠鼻内给药后,该配方合成的LNP表现出改善的上皮和内皮靶向性,且没有明显的促炎特征。
1、CAD部分替代胆固醇合成siRNA CAD-LNPS
本文在临床批准的Onpattro配方配比的基础上,通过三环类抗抑郁药盐酸去甲替林(Nortriptyline hydrochloride,NT) (clogP = 4.51;pKa = 10.1)作为模型CAD化合物,替代摩尔比10%、25 %以及38.5%的胆固醇,配比如图1a所示。
通过透射电镜的结果(图1b)可以看出,CAD以 25%的摩尔比替代胆固醇,所合成的LNP大小和形态均无显著差异,但对LNP的稳定性有积极的影响,在合成后20周内,相对于MC3- LNPs,PDI更低更稳定。然而,包封率会有轻微降低。另外,与最高siRNA浓度的MC3 LNPs相比,MC3- NT(50:25)和MC3- NT (50:10) LNPs针对5-HT2AR激活水平分别降低了39%和33%。在图1g中观察到的拮抗作用比基于理论NT浓度的预期低6倍。总的来说, NT部分取代胆固醇表明,稳定的MC3-NT LNPs可以实现可接受的siRNA包封,并且不会妨碍制剂中CAD的药理活性。
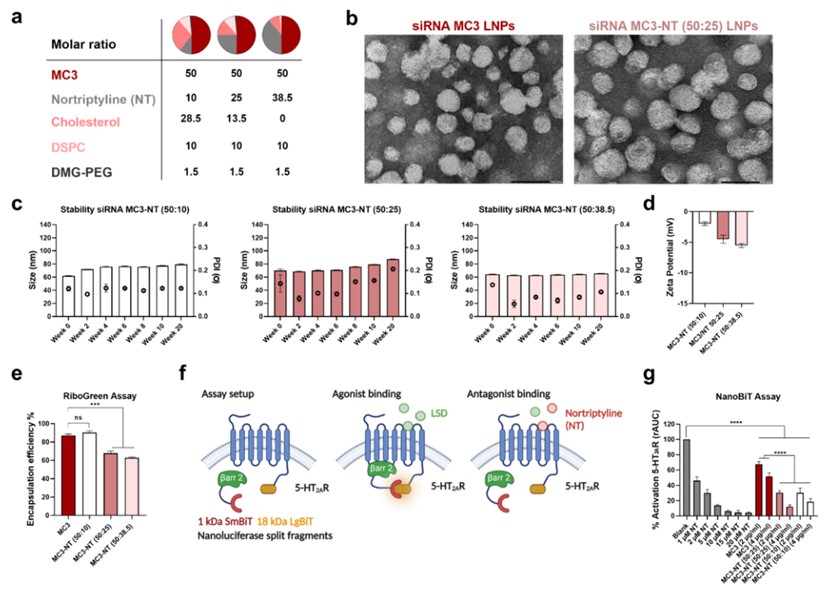
图1 CAD部分替代胆固醇合成CAD-LNPs的物化性质和药理活性:a NT部分替代胆固醇配方对比示意图;b LNP透射电镜对比;c和d 透析后稳定性分析(PBS 4℃保存);e siRNA包封率对比;f NanoBiT系统示意图;g 5-HT2AR激活百分比
2、CAD部分替代胆固醇合成siRNA CAD-LNPS的体外转染效率
本文进一步研究了siRNA负载的CAD-LNPs在局部肺输送中的作用。通过微流技术混合制备稳定的胆固醇含量降低的MC3-NT LNPs,以评估siRNA体外在H1299-eGFP肺上皮细胞中的传递效率。MC3与MC3- NT(50:10)、MC3- NT (50:25) LNPs在细胞内化方面无显著差异,除了siRNA最小剂量 (0.005 μg/mL),如图2a所示。相反,MC3-NT (50:38.5) LNPs含有最大的初始NT并且缺乏胆固醇,显示出细胞摄取受损。尽管在透析期间NT显著丢失,MC3-NT (50:25) LNPs在eGFP敲低方面优于MC3-LNPs,平均需要小至3倍的siRNA剂量才能达到相同的基因沉默水平(图2b),而不会诱导细胞毒性。此外,尽管细胞内siRNA剂量减少了约20倍, MC3-NT (50:38.5) LNPs保持了与MC3 LNPs相当的敲低效率。对这些观察结果的一种可能解释是,CAD-LNP制剂中残留的相对较少的NT在CAD-LNP内吞作用和向溶酶体腔室运输后诱导内溶酶体肿胀和溶酶体膜透化(Lysosomal membrane penetration,LMP),这可能刺激胞质siRNA释放。值得注意的是,仅仅降低胆固醇的比例,不添加NT的MC3 LNPs不增强eGFP沉默。本文还证实,在HT1080-eGFP纤维肉瘤细胞系中,相对于MC3-LNPs,MC3-NT LNPs的eGFP敲低水平更高(50:25)。在HeLa细胞系中,mRNA负载的MC3-NT (50:25) LNPs表现优于MC3-LNPs,在最高mRNA浓度下rMFI值增加了大约3倍。本文发现与未经修饰的LNPs相比,RNA递送的改善可能受到以下因素的影响:(1)由于NT的加入导致LNPs分子组成的变化,(2)在微流控混合过程中NT的存在导致CAD-LNP纳米结构的差异,以及/或(3)由于NT部分的剩余导致LNP性质的变化。需要进行更详细的评估,以进一步阐明这些观测中涉及的生物物理和物理化学参数。
为了评估所开发的CAD-LNPs用于siRNA药物吸入治疗的潜力,本文在人原代支气管上皮细胞(MucilAir)的产生粘液的气液界面(ALI)模型中研究了MC3-和MC3- NT(50:25) LNP的递送,使用雾化将LNPs沉积在细胞上。雾化后,两种LNP的流体动力学尺寸保持不变(图2c)。吸入纳米药物最重要的细胞外生理屏障之一是排列在支气管上皮上的黏液层。为了评估黏液的影响,本研究在MucilAir ALI培养液雾化24 h后,用相同siRNA剂量(0.5 μg/mL)量化了cy5 -siRNA负载的MC3-NT(50:25)和MC3-LNPs的细胞内化(图2d)。平均而言,MC3和MC3- NT (50:25) LNPs均可到达50%的Cy5+支气管上皮细胞。这表明雾化LNPs的很大一部分可以穿过黏液层与下层上皮细胞相互作用。据报道,黏液网状网络的平均孔径在100到200 nm之间,超过了负载siRNA的LNPs的水动力直径。然而,共聚焦成像也清楚地显示了LNPs层状分布在上皮细胞表面的存在,这可能是粘液包裹的结果(图2f)。此外,LNP暴露后,MucilAir纤毛细胞的跳动频率(CBF)和经上皮电阻(TEER),即纤毛清除功能指标和细胞屏障完整性指标,均无显著变化(图2e)。乳酸脱氢酶(LDH)测定证实MC3-NT (50:25) LNP雾化在MucilAir ALI培养物上没有细胞毒性。综上所述,雾化的MC3-NT CAD-LNPs可以穿过粘液屏障到达(产生粘液的)原代支气管上皮细胞。
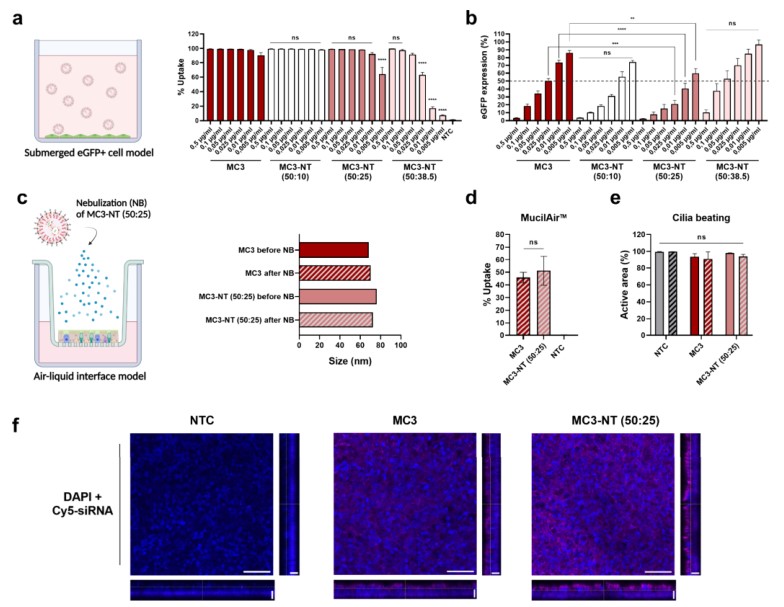
图2 siRNA CAD-LNPs在浸入式H1299-eGFP细胞系中的胞质递送和在人气液界面支气管上皮细胞模型中的粘液穿越:a细胞摄取;b 不同siRNA浓度的MC3-NT(50:10?50:25?50:38.5)LNPs对H1299-eGFP肺上皮细胞系的eGFP沉默作用;c和d 雾化对Cy5-siRNA MC3-NT(50:25)和MC3-LNP在人原代支气管上皮细胞(MucilAir,上皮细胞)气-液界面(ALI)模型中的传递的影响。e LNP对上皮细胞纤毛跳动的影响;f 用MC3-NT(50:25)和MC3-LNPs包封Cy5-siRNA(洋红色),转染24 h后固定MucilAir组织的代表性正交共聚焦图像。
3、小结
总体而言,本研究表明CAD-LNPs是一种稳定的RNA递送平台,可用于治疗包括呼吸系统疾病在内的各种疾病的药物联合方案。稳定的CAD- LNPs可以形成具有常规理化性质和不同siRNA包封率的结构。用CAD部分替代MC3-LNPs中的胆固醇,可提高细胞质siRNA的递送,同时CAD的药理活性得以维持,为药物联合治疗提供了机会。最后,CAD-LNP平台在吸入治疗中也有重要的价值。MC3-NT LNPs在人原代产生黏液的空气-液体界面(ALI)模型上,雾化后能够穿过黏液层到达下层上皮细胞,突破药物肺给药的主要障碍。与未经修饰的MC3-LNPs相比,经鼻给药MC3-NT,特别是MC3-Fluox LNPs可以向小鼠肺上皮和内皮细胞传递更大剂量的siRNA,且在小鼠中没有引起明显的促炎反应。
参考文献:
Selective Replacement of Cholesterol with Cationic Amphiphilic Drugs Enables the Design of Lipid Nanoparticles with Improved RNA Delivery[J].Nano Letters, 2024, 24(10):2961-2971.DOI:10.1021/acs.nanolett.3c03345.
铭汰Microflow系列微流控纳米药物递送平台

【CRO/CMO】纳米药物研发、制造与生产外包
随着纳米技术的不断发展,纳米药物在医药领域的应用越来越广泛,尤其在基因治疗,肿瘤靶向等方面显现了不可替代的优势。锘海生物科学为科研工作者和企业提供全面的纳米药物制备、生产及检测服务,囊括了纳米药物研发过程中,从处方筛选到制剂表征的全线过程。为客户简化流程,节约时间成本,同时提供高质量的数据分析与技术支持服务。
技术服务方案选择
◆ 纳米颗粒制备 ◆
客户确定载体和API以及已有的制备protocol,锘海为您提供纳米制剂制备服务,同时检测颗粒的粒径和包封率。
◆ 科研课题外包 ◆
针对科研客户,锘海提供相关课题的完全外包服务。根据您选择的载体和API,帮助您优化和确定处方并完成制备纳米制剂,提供检测报告和protocol。利用锘海纳米制备核心技术平台,提供一站式服务,让您花同样的时间得到多的结果,减少由于技术瓶颈和人员变化带来的实验波动。助您在短的时间,发出高分的文章!
◆ 企业研发与生产 ◆
针对企业客户,锘海提供从载体选择到纳米制剂制备服务。从载体的筛选,处方优化,以及扩大生产(cGMP级别)锘海提供完整的解决和服务方案。缩短研发项目周期,减少科研与生产人力成本,解决无法扩大生产的技术瓶颈!