- 首页
- 关于我们
-
产品中心
- 光片显微镜系列
- LS-COMPACT光片显微镜 LS18平铺光片显微镜 锘海组织透明化底透台 透明度检测仪 组织透明化染色仪 高频震动切片机 活体循环系统 SHIELD 透明化试剂 AMIRA三维视图和分析软件
- 透明化试剂盒系列
- 组织透明化试剂盒(亲水型) 组织膨胀试剂盒 胚胎透明化试剂盒 增强型组织透明化试剂盒 细胞膨胀试剂盒 皮肤透明化试剂盒 组织切片透明&膨胀试剂盒(试用装)
- 组织透明化及成像服务
- 一站式科研服务——组织透明化、免疫染色、3D成像、数据分析及存储
- 小动物活体成像
- 小动物近红外二区成像
- 纳米药物制备系统/服务
- 微流控纳米药物递送平台 纳米药物载体合成服务
- 生物3D打印设备
- RegenHU生物3D打印机
- 活体多光子及高分辨显微成像系统
- 高分辨率显微成像系统 双光子荧光寿命计数系统 活体多光子显微成像系统
- 试剂耗材
- 抗体系列产品 GATTA 显微镜纳米标尺 RISystem小鼠骨钉 Cellendes细胞水凝胶
- 小动物灌注/灌流设备
- 小动物灌注系统 灌流设备及附件
- 类器官3D细胞培养
- 锘海类器官、3D细胞培养系统
-
应用案例
- 成像视频
- 成像视频
- 成像图片
- 成像图片
- 新闻资讯
- 联系我们
mRNA-LNPs疫苗仍需考虑的关键问题及3D生物打印技术的应用
发布日期:2022/12/8 16:41:00
BioNTech/Pfizer和Moderna的疫苗主要由核酸脂质纳米粒(LNPs)包裹的mRNA组成。纳米药物递送平台的模块化和产业化并非短时间内完成的,而是数十年来密集研究的产物,在设计最佳的mRNA-LNPs疫苗时,需要考虑诸多因素。本文作者简要概述了mRNA-LNPs疫苗递送系统仍须考虑的关键问题,接着,对3D生物打印组织上的疫苗验证提出了自己的看法。与动物模型相比,3D生物打印验证系统在未来会承担更快、更低成本、更有预测性的疫苗测试任务。
LNPs的疫苗递送系统仍须考虑的关键问题:
1.脂质成分替代
大多数情况下,治疗靶点决定给药途径的选择,Onpattro?的脂质成分专门设计用于静脉给药后的肝细胞靶向,其中,阳离子脂质作用于siRNA的包裹与释放,PEG脂质有助于增加药物的血液循环时间。然而,这两种脂质成分也都有各自的缺点。例如,阳离子脂质易受温度和pH依赖性水解的影响,导致纳米粒子的不稳定,而高浓度的PEG脂质会阻止RNA进入细胞,其引发的PEG免疫反应也会加速血液清除现象。
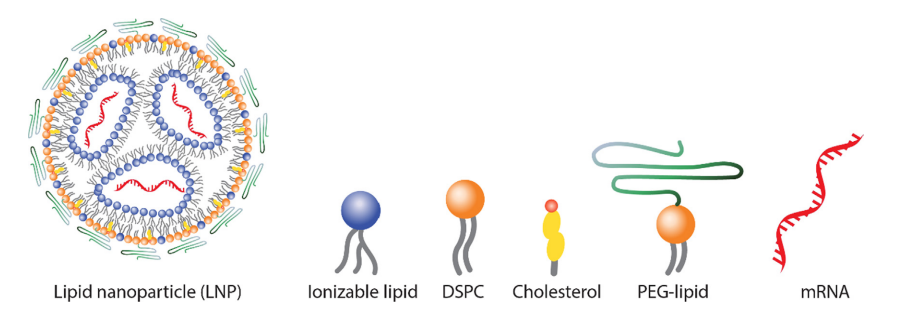
图1.各脂质成分及LNP示意图
对于mRNA-LNPs疫苗,肌肉注射是最常见的给药途径,这允许LNPs扩散到淋巴,在淋巴中,mRNA-LNPs疫苗可以直接接触APCs,不存被免疫细胞清除的风险,这意味着通过肌肉给药时,LNPs中的阳离子脂质和PEG脂质为非必须成分。因此,未来的研究旨在发掘阳离子脂质和PEG脂质的替代材料,以获取更好的疫苗疗效,如可对两性离子材料和人工蛋白涂层等进行研究。
2.mRNA-LNPs真实结构探究
纳米尺度的结构排列是决定核酸功能传递的关键因素,不同形态的纳米粒子其转染性能差异巨大。到目前为止,对于LNPs中包裹mRNA的确切排列还没有较为透彻的研究,大部分的信息都是通过siRNA-LNPs系统获得的。然而,mRNA至少比siRNA大100倍,从siRNA-LNPs的结构中获得的经验是否以及在多大程度上适用于mRNA-LNPs仍存在争议。

图2.LNP不同结构排列示意图
如能更好地理解纳米粒子结构与活性之间的关系,则可更快速的优化mRNA-LNPs并创建有效的免疫传递系统。在这方面,定量结构-活性关系(QSAR)方法可以用于预测mRNA-LNPs的合成特性与其在细胞水平上的作用机制之间的关系。QSAR方法假设具有相似合成特性的LNPs将与细胞发生类似的相互作用,从而引发类似的生理反应(例如,蛋白的表达和抗体的产生)。作者预计QSAR研究将使体外生物活性预测成为可能,并加速mRNA-LNPs疫苗的优化过程。
3D生物打印组织上的疫苗验证
给药系统的验证需要建立适当的体外模型进行配方筛选。虽然二维细胞培养系统在药理研究方面发挥着关键作用,但其缺乏由相邻细胞、分子梯度和细胞外基质(ECM)等组成的复杂组织结构,所得的研究结果很难转化至体内生理系统。3D生物打印则能创建更接近生理环境的立体模型,使用3D细胞培养也有利于通过多种荧光标记或其他旨在跟踪免疫细胞之间相互作用的技术来跟踪细胞与细胞之间的动态相互作用。
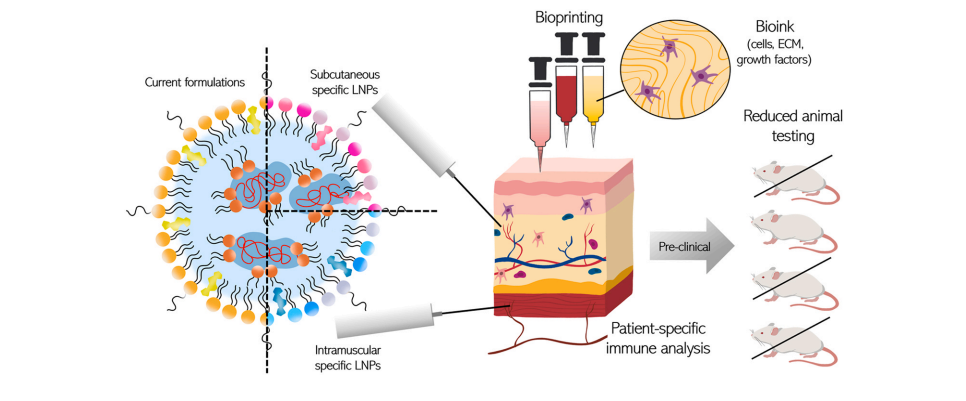
图3.在3D生物打印组织中进行LNPs特异性递送试验
近些年来,仿生3D组织模型的开发取得了诸多进展,肺部组织的3D模型已用于器官功能衰竭的研究、完整的具有免疫能力的3D皮肤也已用于疫苗反应分析。在减少试验动物数量的同时,3D组织模型还能帮助人们从根本上了解免疫激活效力与给药途径不同带来的差异,这在疫情大流行的背景下显得非常有必要。
小 结
在应对疫情方面,mRNA-LNPs疫苗已取得了很好的成绩,但仍有较大的改进空间。不断的优化载体成分与配比,摸清LNPs纳米尺度的排布规律,方能积累更多的可用经验,为LNPs其他领域的治疗提供新动力。而3D生物打印则为疫苗的测试提供了全新的路径,相信在未来几年,3D生物打印定能提供更快、更有预测性的疫苗测试能力。
注:文章内容多来自文献参考,文献题为“Principles for optimization and validation of mRNA lipid nanoparticle vaccines against COVID-19 using 3D bioprinting”,如需了解更多内容,可直接查阅原文献。
参考文献:
[1] Papi M, Pozzi D, Palmieri V, Caracciolo G. Principles for optimization and validation of mRNA lipid nanoparticle vaccines against COVID-19 using 3D bioprinting. Nano Today. 2022 Apr;43:101403. doi: 10.1016/j.nantod.2022.101403. Epub 2022 Jan 21. PMID: 35079274; PMCID: PMC8776405.
[2] Hald Albertsen C, Kulkarni JA, Witzigmann D, Lind M, Petersson K, Simonsen JB. The role of lipid components in lipid nanoparticles for vaccines and gene therapy. Adv Drug Deliv Rev. 2022 Sep;188:114416. doi: 10.1016/j.addr.2022.114416. Epub 2022 Jul 3. PMID: 35787388; PMCID: PMC9250827.
[3] Tenchov R, Bird R, Curtze AE, Zhou Q. Lipid Nanoparticles─From Liposomes to mRNA Vaccine Delivery, a Landscape of Research Diversity and Advancement. ACS Nano. 2021 Nov 23;15(11):16982-17015. doi: 10.1021/acsnano.1c04996. Epub 2021 Jun 28. PMID: 34181394.
