常规的组织学检查通常使用冷冻或石蜡包埋的样本切片,微米级别厚度的组织切片允许对单个细胞进行标记及表征,但却无法探知生物样本的三维特性。切片分析只对病理样本的局部进行了探测研究,整个病理组织中,有相当大部分的信息仍未被探索。随着组织透明化技术的发展与光片显微镜的诞生,我们终于可以对完整样本进行完整的成像表征。最近发表在Nature Reviews Cancer的一篇综述中[1]总结了组织透明化、成像技术及3D成像的新应用等。

组织透明化方法在近十年内迅速发展,各种化合物的联合使用已被广泛用于减少光散射和光吸收,并增加光学显微镜在成像中的成像深度。虽然组织透明化最初由神经科学家用于描绘小鼠中枢和外周的神经系统,而近几年的研究表明,对于组织的三维成像也可助力发育生物学、免疫学、肿瘤学和肿瘤机理等多种学科。例如肿瘤研究中,三维荧光成像已被用于评估肿瘤迁移性、肿瘤组织结构、细胞异质性、表征肿瘤微环境和评估肿瘤模型的治疗反应等。作者首先对各种透明化方法的特点进行了比较与介绍,肿瘤因其异质性及致密的结构首先需选择适当的透明化方式。接下来,作者介绍了3D成像在肿瘤研究中的应用:1.成像并定量:2D成像无法避免因切片带来的数据缺失,3D成像则可以很直接的进行数据定量[2];

2.肿瘤结构:3D成像有助于从细胞转化、细胞骨架等肿瘤模型中进行发生、发展分析[3];
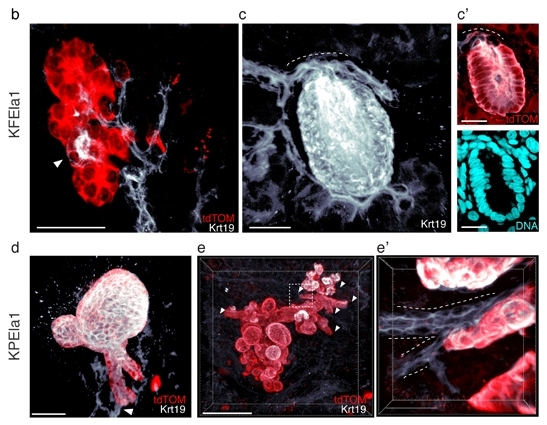
3.脉管系统:脉管系统与肿瘤进展及侵袭性相关,3D成像有助于评估抗血管生成的治疗反应[4];
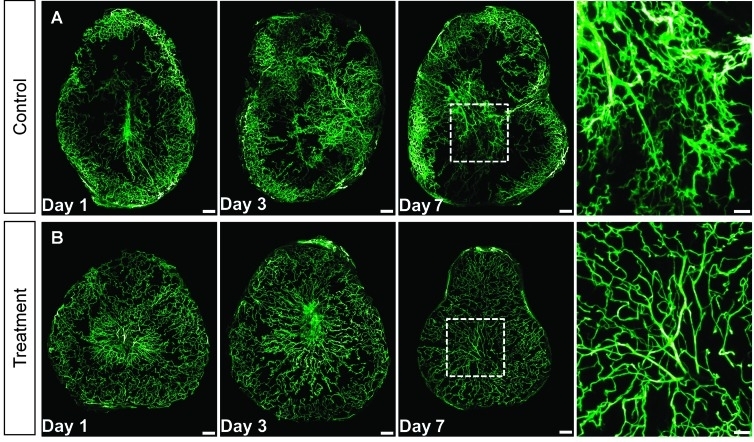
此外,对完整组织的3D成像也有助于对于肿瘤的转移评估、深入探索肿瘤微环境;肿瘤侵袭、传播与耐药性相关的病理研究;3D组织病理学研究等。[1] Almagro J, Messal HA, Zaw Thin M, van Rheenen J, Behrens A. Tissue clearing to examine tumour complexity in three dimensions. Nat Rev Cancer. 2021 Jul 30. doi: 10.1038/s41568-021-00382-w. Epub ahead of print. PMID: 34331034.[2] Wei M, Shi L, Shen Y, Zhao Z, Guzman A, Kaufman LJ, Wei L, Min W. Volumetric chemical imaging by clearing-enhanced stimulated Raman scattering microscopy. Proc Natl Acad Sci U S A. 2019 Apr 2;116(14):6608-6617. doi: 10.1073/pnas.1813044116. Epub 2019 Mar 14. PMID: 30872474; PMCID: PMC6452712.[3] Messal HA, Alt S, Ferreira RMM, Gribben C, Wang VM, Cotoi CG, Salbreux G, Behrens A. Tissue curvature and apicobasal mechanical tension imbalance instruct cancer morphogenesis. Nature. 2019 Feb;566(7742):126-130. doi: 10.1038/s41586-019-0891-2. Epub 2019 Jan 30. PMID: 30700911; PMCID: PMC7025886.[4] Dobosz M, Ntziachristos V, Scheuer W, Strobel S. Multispectral fluorescence ultramicroscopy: three-dimensional visualization and automatic quantification of tumor morphology, drug penetration, and antiangiogenic treatment response. Neoplasia. 2014 Jan;16(1):1-13. doi: 10.1593/neo.131848. PMID: 24563615; PMCID: PMC3924547.锘海一站式科研服务,让科研变得更简单!
锘海生命科学为广大客户提供专业的生物组织透明化、免疫染色、平铺光片显微镜3D荧光成像、数据分析、数据存储等一站式科研服务,旨在通过快速、多样化的科研服务为每一位生命科学工作者提供个体化/定制化的解决方案。
请联系 021-37827858、13818273779(微信同号)






