在前几期的内容当中,我们重点介绍了设备的参数调控,样品的后处理等。相信广大用户对我们的设备已经越来越熟悉了。本期,我们暂不谈纳米药物制备系统本身,而是介绍一下其应用最多的一个方向——mRNA疫苗。下面,小编将从(mRNA治疗优势、mRNA疫苗开发过程、LNP系统有效递送需克服的障碍及mRNA治疗面临的挑战)四个方面浅谈一下对mRNA疫苗开发的了解。mRNA治疗优势:
1、增强靶向性,对传统药物疗效不佳的疾病产生突破性的进展。
2、RNA药物不需要核递送和转录,使mRNA成为基因治疗的简单解决方案。3、mRNA的作用是短暂的,其本质上比整合到基因组中的系统更安全。
基因治疗过程
mRNA疫苗开发过程:
2、抗体基因测序,从成千上万个抗体中挑出潜在的优良抗体基因?(针对熟知的特定疾病,可从已有的抗体数据库直接挑选潜在优良基因,节省抗体取得及基因测序步骤。)3、抗体基因回溯到蛋白质,完成排位后,进行病毒表面蛋白的识别与结合,观察每一个抗体之间结合能力?阻断能力?更高的目标:利用晶体学等方法,解析出病毒表面刺突与细胞表面蛋白(“钥匙”和“锁”)之间的结构基础?
(LNP核酸递送系统在以往的推文中已有详细的介绍,简单回顾一下其脂质载体包含的四种成分:阳离子脂质,胆固醇,中性脂质,PEG脂质。)
1、在体液中保护mRNA以防止其被核酸酶降解。阳离子脂质以静电吸附的方式将有效成分mRNA进行包裹,保护其不被降解。
2、在给药后LNP应避免被吞噬细胞清除。PEG分子的修饰可有效避免LNP被肾脏?巨噬细胞清除?
3、LNP递送系统必须能够到达目标细胞并且被细胞摄入。胆固醇的加入增强LNP膜的稳定性与融合性,促进mRNA胞内摄入和胞质进入?
4、在被摄入细胞后,载运的mRNA需要能够被释放出内体进入细胞质并翻译。mRNA的释放和蛋白表达过程,严重依赖于LNP颗粒大小和细胞类型。在制备样品时,可通过调节微流控设备的流速及流速比等参数有效控制颗粒直径,加速蛋白表达。

mRNA治疗面临的挑战
1、除肝脏以外器官的靶向能力成为mRNA药物研发市场较难越过的门槛。PEG分子易于修饰,可通过连接特定配体的方式使得LNP具有靶向性,但靶向配体的探索需耗费大量时间。
2、多抗原mRNA疫苗的制备需要大量的LNPs,而LNPs具有佐剂特性,其安全性和耐受性有待长期验证。
3、外源mRNA产生强烈的免疫应答,抑制抗原的表达。需要通过LNP粒径调控或mRNA中碱基比例调控来降低免疫原性。
结论:mRNA行业拥有巨大的科研与市场前景,其供应链平台,修饰、递送平台仍处于发展阶段。具有“先发优势”的企业少之又少,尽早布局有望弯道超车。
纳米药物制备系统:

应用范围:
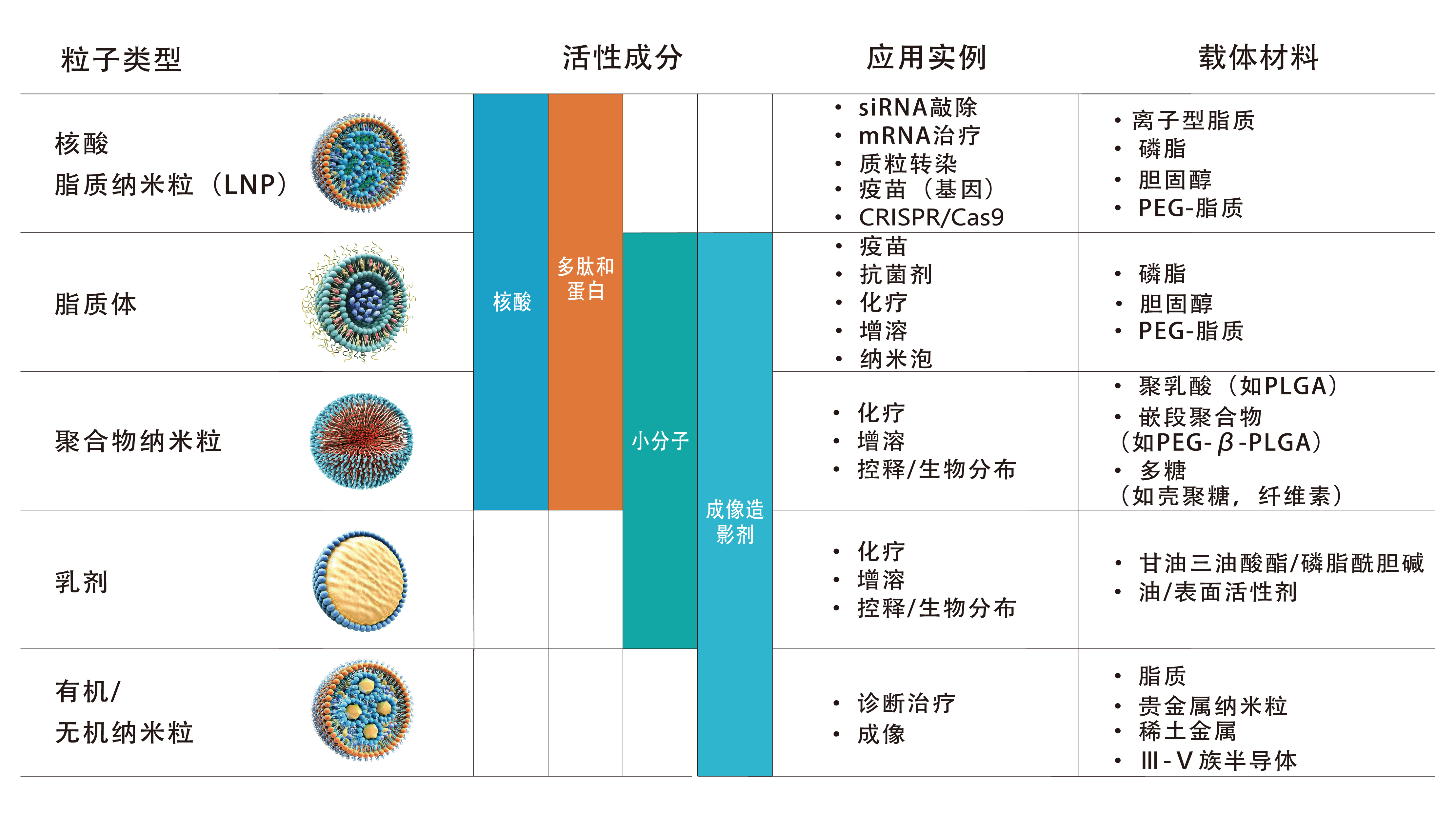
请联系021-37827858 或 13818273779(微信同号)点击以下链接,查看往期回顾
核酸脂质纳米粒科普——浅谈仪器参数对结果的影响
核酸脂质纳米粒科普——超滤管规格
核酸脂质纳米粒(LNP)科普 —— 组成成分及作用





